Anh hay Việt Nam là nước đầu tiên phê duyệt thuốc uống điều trị COVID-19 đang gây sốt trên thế giới?
Khoa học - công nghệ - Ngày đăng : 18:14, 04/11/2021
Theo nhiều hãng tin quốc tế, Anh là quốc gia đầu tiên trên thế giới phê duyệt molnupiravir, loại thuốc kháng vi rút SARS-CoV-2 có khả năng thay đổi cuộc chơi do hãng dược Merck & Co (Mỹ) và Ridgeback Biotherapeutics (Đức) cùng phát triển, nhằm thúc đẩy cuộc chiến chống lại đại dịch.
Thế nhưng hôm 7.10, tại Việt Nam, Bộ Y tế chính thức đưa thuốc molnupiravir 400mg vào phác đồ điều trị COVID-19, cùng với remdesivir và favipiravir. Molnupiravir được Bộ Y tế hướng dẫn dùng cho bệnh nhân COVID-19 nhẹ, liều dùng theo đề cương thử nghiệm lâm sàng đã được phê duyệt, chống chỉ định với phụ nữ có thai 3 tháng đầu, phụ nữ đang có kế hoạch có thai. Dù vậy, Việt Nam chỉ mới thử nghiệm chứ chưa cấp phép có điều kiện cho molnupiravir như Anh.
Việt Nam đã nhận số lượng lớn molnupiravir qua nhập khẩu và được tài trợ. Nhiều bệnh nhân COVID-19 ở Việt Nam, đặc biệt là TP.HCM, đã được nhận thuốc này để sử dụng tại nhà.
Từ tháng 8 vừa qua, molnupiravir đã được Sở Y tế TP.HCM sử dụng có kiểm soát để điều trị cho bệnh nhân COVID-19 có triệu chứng nhẹ với hướng dẫn toa thuốc điều trị tại nhà dành cho người lớn là 800 mg molnupiravir/ngày chia thành 2 lần, dùng trong 5 ngày liên tục. Molnupiravir được dùng qua đường uống kết hợp một số loại vitamin và thuốc chống đông máu.
Theo PGS.TS.BS Nguyễn Thanh Hiệp, Hiệu trưởng Trường Đại học Y khoa Phạm Ngọc Thạch (TP.HCM), việc sử dụng molnupiravir trong điều trị COVID-19 đã cứu sống kịp thời nhiều bệnh nhân F0 tại nhà và các khu cách ly tập trung.
Đã có ít nhất 10 nước, trong đó có 8 quốc gia và vùng lãnh thổ khu vực châu Á - Thái Bình Dương (New Zealand, Úc, Hàn Quốc, Singapore, Thái Lan, Malaysia, Philippines, Đài Loan) đặt mua molnupiravir.
Các chuyên gia cho rằng các quốc gia và vùng lãnh thổ này không muốn lịch sử lặp lại khi năm 2020, họ đã chậm trễ trong việc tìm kiếm vắc xin và không muốn lại rơi vào cái bẫy trước đây khi các nước giàu gom vắc xin, gây khan hiếm nguồn cung.

Ở Anh, molnupiravir được cấp phép cho người lớn từ 18 tuổi trở lên có kết quả xét nghiệm dương tính với COVID-19 và có ít nhất một yếu tố nguy cơ phát triển bệnh nặng, chẳng hạn như béo phì hoặc bệnh tim. Molnupiravir được dự định sử dụng 2 lần/ngày trong 5 ngày cho những bệnh nhân COVID-19 ở nhà có mức độ bệnh nhẹ đến trung bình.
Molnupiravir làm giảm các triệu chứng và tăng tốc độ phục hồi có thể chứng minh một bước đột phá, giúp giảm bớt tình trạng đổ xô vào các bệnh viện và giúp hạn chế sự bùng phát ở các nước nghèo hơn với hệ thống y tế yếu kém. Molnupiravir cũng sẽ củng cố cách tiếp cận theo hai hướng với đại dịch: Điều trị (bằng cách dùng thuốc) và phòng ngừa (chủ yếu thông qua tiêm vắc xin).
Các cơ quan quản lý ở Mỹ, Liên minh châu Âu và nơi khác cũng đang xem xét molnupiravir. Vào tháng trước, Cục Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) đã thông báo rằng sẽ triệu tập một hội đồng gồm các chuyên gia độc lập để xem xét kỹ lưỡng tính an toàn và hiệu quả của thuốc này vào cuối tháng 11.2021.
Nguồn cung cấp ban đầu sẽ có hạn. Merck & Co cho biết có thể sản xuất 10 triệu liệu trình điều trị COVID-19 cho đến cuối năm nay, nhưng phần lớn nguồn cung đó đã được các chính phủ trên toàn thế giới mua.
Vào tháng 10.2021, các quan chức Anh thông báo họ đã mua được 480.000 liệu trình molnupiravir và dự kiến hàng nghìn người Anh dễ bị tổn thương sẽ được tiếp cận với phương pháp điều trị trong mùa đông này thông qua một nghiên cứu quốc gia.
“Hôm nay là một ngày lịch sử với đất nước chúng tôi, vì Anh hiện là quốc gia đầu tiên trên thế giới phê duyệt một loại thuốc kháng vi rút SARS-CoV-2 có thể uống tại nhà”, Bộ trưởng Y tế Anh - Sajid Javid cho biết.
“Chúng tôi đang làm việc với tốc độ nhanh chóng trong toàn chính phủ và với Dịch vụ y tế quốc gia (NHS) để đặt ra kế hoạch triển khai molnupiravir cho bệnh nhân thông qua một nghiên cứu quốc gia càng sớm càng tốt”, ông nói thêm.
Các bác sĩ cho biết việc điều trị COVID-19 bằng molnupiravir sẽ đặc biệt có ý nghĩa với những người không đáp ứng tốt với tiêm vắc xin.
Merck & Co và đối tác Ridgeback Biotherapy đã đề nghị thông quan thuốc với các cơ quan quản lý trên toàn thế giới để điều trị cho người lớn mắc COVID-19 từ nhẹ đến trung bình, những người có nguy cơ mắc bệnh nặng hoặc phải nhập viện. Đó gần giống với nhóm được nhắm mục tiêu điều trị bằng thuốc kháng thể COVID-19 dạng truyền, tiêu chuẩn chăm sóc ở nhiều quốc gia cho những bệnh nhân chưa cần nhập viện.
Merck & Co đã công bố kết quả sơ bộ vào tháng trước cho thấy molnupiravir giúp giảm một nửa số ca nhập viện và tử vong ở những bệnh nhân có các triệu chứng COVID-19 sớm. Kết quả chưa được bình duyệt hoặc công bố trên tạp chí khoa học.
Merck & Co cũng không tiết lộ chi tiết về tác dụng phụ của molnupiravir, ngoại trừ nói rằng tỷ lệ những vấn đề đó là tương tự giữa những người dùng thuốc này và những ai nhận giả dược.
Thuốc nhắm vào một loại enzyme mà vi rút SARS-CoV-2 sử dụng để tự tái tạo, chèn các lỗi vào mã di truyền của nó làm chậm khả năng lây lan và tiếp quản tế bào người. Hoạt động di truyền đó đã khiến một số chuyên gia độc lập đặt câu hỏi liệu molnupiravir có khả năng gây đột biến dẫn đến dị tật bẩm sinh hoặc khối u hay không.
Cơ quan quản lý thuốc và sản phẩm chăm sóc sức khỏe của Anh cho biết khả năng tương tác với DNA và gây đột biến của molnupiravir đã được nghiên cứu rộng rãi, không phát hiện thấy nó có nguy cơ gây nguy hiểm cho con người.
Cơ quan này thông báo: “Các nghiên cứu trên chuột cho thấy molnupiravir có thể gâycác tác động có hại cho con chưa sinh ra nhưng liều lượng này cao hơn so với liều được cung cấp cho con người và những tác động này không được quan sát thấy ở các động vật khác”.
Trong các thử nghiệm của Merck & Co, cả nam giới và phụ nữ đều được hướng dẫn sử dụng biện pháp tránh thai hoặc kiêng quan hệ tình dục. Phụ nữ mang thai bị loại khỏi nghiên cứu. Merck & Co đã tuyên bố rằng thuốc này an toàn khi sử dụng theo chỉ dẫn.
Molnupiravir ban đầu được nghiên cứu như một liệu pháp điều trị cúm tiềm năng với sự tài trợ của chính phủ Mỹ. Năm ngoái, các nhà nghiên cứu tại Đại học Emory đã quyết định sử dụng lại loại thuốc này như một phương pháp điều trị COVID-19 tiềm năng. Sau đó, họ đã cấp phép loại thuốc này cho Ridgeback Biotherapeutics và Merck & Co.
Tuần trước, Merck & Co đã đồng ý cho phép các hãng dược khác sản xuất molnupiravir, trong động thái nhằm giúp hàng triệu người ở các quốc gia nghèo hơn được tiếp cận. Tổ chức Sáng chế Thuốc, một nhóm do Liên Hợp Quốc hậu thuẫn, cho biết Merck & Co sẽ không nhận được tiền bản quyền theo thỏa thuận chừng nào Tổ chức Y tế Thế giới (WHO) coi COVID-19 là trường hợp khẩn cấp toàn cầu.
Tuy nhiên, thỏa thuận này đã bị một số nhà hoạt động chỉ trích vì loại trừ nhiều quốc gia thu nhập trung bình có khả năng thực hiện hàng triệu ca điều trị, trong đó có Brazil và Trung Quốc.
Các chuyên gia vẫn khen ngợi Merck & Co vì đã đồng ý chia sẻ rộng rãi công thức của mình và hứa sẽ giúp bất kỳ công ty nào cần trợ giúp về công nghệ trong việc sản xuất thuốc của họ - điều mà ít nhà sản xuất vắc xin COVID-19 nào đồng ý.
Tiến sĩ Mohga Kamal-Yanni, cố vấn y tế cấp cao của Liên minh vắc xin Nhân dân, cho biết: “Không giống như việc phân phối vắc xin COVID-19 không đồng đều một cách kỳ lạ, các nước nghèo nhất sẽ không phải chờ đợi ở phía sau hàng đợi để mua molnupiravir. Ít hơn 1% vắc xin COVID-19 trên thế giới đã được chuyển đến các nước nghèo và các chuyên gia hy vọng các phương pháp điều trị dễ dàng phân phối sẽ giúp họ kiềm chế đại dịch”.
Trước đây, Merck & Co đã công bố các hợp đồng cấp phép với một số nhà sản xuất thuốc generic của Ấn Độ để sản xuất các phiên bản giá rẻ hơn của molnupiravir cho các nước đang phát triển.
Theo báo cáo, Mỹ đã trả khoảng 700 USD cho mỗi liệu trình của molnupiravir cho khoảng 1,7 triệu lần điều trị. Merck & Co cho biết có kế hoạch sử dụng chiến lược định giá theo từng cấp độ cho các nước đang phát triển. Một đánh giá của Đại học Harvard (Mỹ) và Cao đẳng Hoàng gia London (Anh) ước tính loại thuốc này có giá khoảng 18 USD để sản xuất.
Theo Giáo sư Matthias Götte của Đại học Alberta (Canada), chỉ nên coi molnupiravir là một lựa chọn nữa trong phòng chống COVID-19 thay vì giải pháp cuối cùng và vắc xin vẫn phải ưu tiên hàng đầu. Hơn nữa, molnupiravir vẫn có thể sử dụng được cho những người đã tiêm vắc xin nhiễm vi rút SARS-CoV-2, nên đây sẽ làlựa chọn bổ sung để gia tăng khả năng chống dịch, đặc biệt áp dụng với những ai chưa có khả năng hoặc không đủ điều kiện để tiêm vắc xin.
Các phương pháp điều trị COVID-19 khác, bao gồm steroid và kháng thể đơn dòng, được thực hiện bằng cách tiêm hoặc truyền và chủ yếu dành cho bệnh nhân nhập viện.
Molnupiravir và các loại thuốc trong phác đồ điều trị COVID-19 của Việt Nam
Ngoài molnupiravir, Việt Nam còn đưa một số thuốc vào phác đồ điều trị. Trong đó có các thuốc dùng trong tình huống khẩn cấp đã được công nhận trên thế giới như remdersivir, IL-6; thuốc kháng đông, kháng viêm sử dụng sớm đã giúp kiểm soát được các trường hợp nhiễm SARS-CoV-2 tại nhà, các cơ sở thu dung y tế, tại các bệnh viện…
Trong hướng dẫn chẩn đoán, điều trị COVID-19 đã ban hành, Bộ Y tế bổ sung kháng vi rút, thuốc kháng thể kháng vi rút, thuốc ức chế IL-6 nếu đã được cấp phép sử dụng khẩn cấp tại ít nhất một nước trên thế giới. Trong đó, 3 thuốc kháng vi rút được đưa vào hướng dẫn, gồm remdesivir dùng cho bệnh nhân có triệu chứng trung bình, nặng; favipiravir dùng cho bệnh nhân không triệu chứng, triệu chứng nhẹ trung bình; molnupiravir dùng cho bệnh nhân mức độ nhẹ.
"Các thuốc kháng vi rút này giúp giảm tải lượng vi rút, chứ không phải là diệt vi rút", PGS.TS Lương Ngọc Khuê, Cục trưởng Cục Quản ký khám chữa bệnh, nói hôm 7.10.
Favipiravir 200mg
Thuốc dùng cho bệnh nhân nhẹ, chống chỉ định với phụ nữ có thai hoặc đang có kế hoạch có thai, người đang cho con bú, người dưới 18 tuổi, suy gan, suy thận nặng.
Về liều dùng, ngày đầu uống 2 lần, mỗi lần 1.600 mg; các ngày sau mỗi ngày uống 2 lần, mỗi lần uống 600mg. Thời gian điều trị 7-14 ngày. Bệnh nhân COVID-19 dùng thuốc chú ý ít nhất hai ngày đầu do có thể gây rối loạn tâm thần. Người tiền sử gout càng cần chú ý theo dõi sức khỏe khi dùng thuốc vì có thể tăng acid uric và làm nặng thêm bệnh.
Favipiravir do hãng Fujifilm sản xuất, được Nhật Bản phê duyệt vào năm 2014 để điều trị bệnh cúm. Thuốc có cơ chế hoạt động tương tự remdesivir, ngăn chặn quá trình nhân lên của vi rút SARS-CoV-2, loại bỏ vi rút khỏi đường thở. Hiện favipiravir được sử dụng tại một số nước như Nhật Bản, Nga, Thái Lan...
Theo Bộ Y tế, favipiravir có tác dụng ngăn ngừa bệnh tiến triển nghiêm trọng, giúp bệnh nhân phục hồi nhanh hơn và giảm gánh nặng điều trị bằng cách rút ngắn thời gian nằm viện. Thuốc giúp sớm loại bỏ vi rút để hạn chế lây nhiễm bệnh trong cộng đồng.
Remdesivir
Thuốc chỉ định với bệnh nhân nội trú khởi phát bệnh chưa quá 10 ngày có suy hô hấp phải thở oxy, thở oxy lưu lượng dòng cao (HFNC), hoặc thở máy không xâm nhập. Thuốc này được Bộ Y tế khuyến cáo phối hợp với thuốc corticoid (ưu tiên dexamethason).
Nhóm bệnh nhân được dùng remdersivir là người trên 65 tuổi, người có bệnh nền, người béo phì (BMI > 25). Thuốc không sử dụng cho người bệnh COVID-19 cần thở máy xâm nhập, can thiệp ECMO. Các trường hợp đã được điều trị bằng remdesivir trước khi thở máy xâm nhập hoặc ECMO thì có thể tiếp tục dùng cho đủ liệu trình.
Theo Thứ trưởng Bộ Y tế Nguyễn Trường Sơn, "cơ bản thuốc này đã góp phần điều trị giảm được nồng độ vi rút và giảm được tỷ lệ tử vong với bệnh nhân COVID-19".
Remdesivir do Gilead Sciences sản xuất, ban đầu được thử nghiệm để điều trị Ebola và viêm gan C nhưng không thành công. Trong dịch COVID-19, các nhà khoa học phát hiện nó có thể ngăn vi rút SARS-CoV-2 sinh sôi trong tế bào. Thử nghiệm lớn sau đó cho thấy remdesivir giúp giảm thời gian hồi phục của người bệnh từ 15 ngày xuống còn 11 ngày.
Remdesivir được FDA phê duyệt khẩn cấp tháng 10.2020 để điều trị bệnh nhân COVID-19. Remdesivir có tác dụng rút ngắn thời gian hồi phục và giảm tỷ lệ tử vong ở bệnh nhân diễn tiến nặng.
Việt Nam cần chú ý hai loại thuốc có tiềm năng điều trị COVID-19
Thuốc chữa trầm cảm giá rẻ làm giảm nguy cơ phải nhập viện do COVID-19
Fluvoxamine, loại thuốc chữa trầm cảm giá rẻ, đã làm giảm nguy cơ phải nhập viện ở những người trưởng thành mắc COVID-19 trong một nghiên cứu tìm kiếm các loại thuốc hiện nay có thể được dùng điều trị bệnh này.
Các nhà nghiên cứu đã thử nghiệm fluvoxamine được sử dụng điều trị chứng trầm cảm và rối loạn ám ảnh cưỡng chế vì có tác dụng giảm viêm, hứa hẹn có tiềm năng điều trị COVID-19 trong các nghiên cứu nhỏ hơn.
Các nhà nghiên cứu đã chia sẻ kết quả với Viện Y tế Quốc gia Mỹ, nơi đưa ra các hướng dẫn điều trị và họ hy vọng sẽ nhận được khuyến nghị của WHO.
“Nếu WHO khuyến nghị điều này, bạn sẽ thấy nó được áp dụng rộng rãi. Chúng tôi hy vọng loại thuốc này có thể cứu sống được nhiều người”, đồng tác giả nghiên cứu, Tiến sĩ Edward Mills thuộc Đại học McMaster ở thành phố Hamilton (tỉnh Ontario, Canada) cho biết và nhấn mạnh rằng nhiều nước nghèo có sẵn loại thuốc này.
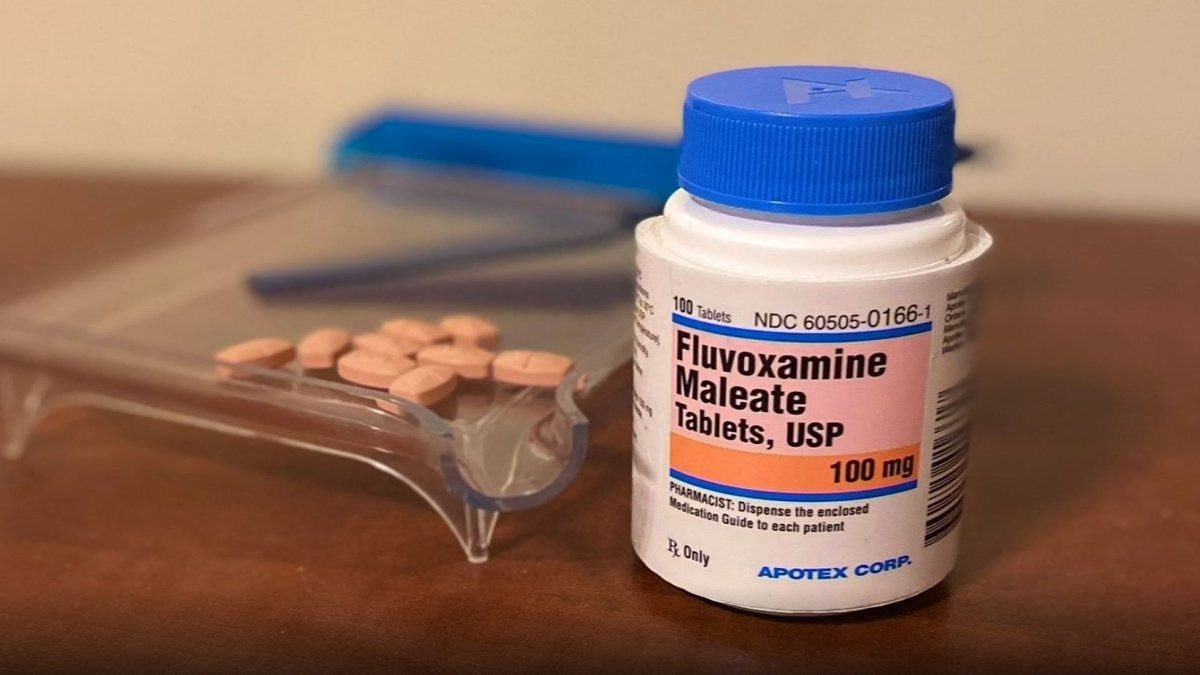
Fluvoxamine có giá 4 USD cho một đợt điều trị COVID-19. Để so sánh với phương pháp điều trị bằng kháng thể đơn dòng có giá khoảng 2.000 USD và thuốc kháng vi rút SARS-CoV-2 của hãng dược Merck là khoảng 700 USD cho mỗi liệu trình thì fluvoxamine giá rẻ hơn nhiều. Một số chuyên gia dự đoán các phương pháp điều trị khác nhau cuối cùng sẽ được sử dụng kết hợp để chống lại vi rút SARS-CoV-2.
Các nhà nghiên cứu đã thử nghiệm fluvoxamine ở gần 1.500 người dân Brazil gần đây đã mắc COVID-19, những người có nguy cơ bị nặng vì có các bệnh nền chẳng hạn tiểu đường. Khoảng một nửa dùng thuốc fluvoxamine tại nhà trong 10 ngày, số còn lại dùng giả dược. Họ được theo dõi trong 4 tuần để xem ai sẽ phải nhập viện.
Trong nhóm dùng thuốc fluvoxamine, chỉ 11% cần nhập viện hoặc thời gian điều trị kéo dài, so với 16% những người dùng giả dược.
Kết quả nghiên cứu được công bố trên tạp chí Lancet Global Heath ngày 28.10 gây chú ý đến mức các chuyên gia độc lập theo dõi nghiên cứu khuyến cáo nên dừng nghiên cứu sớm vì kết quả đã rất rõ ràng.
Các vấn đề chưa được làm rõ về phương pháp này là mức độ liều lượng, liệu những bệnh nhân COVID-19 có nguy cơ thấp hơn cũng có thể được điều trị hay không và liệu loại thuốc này có nên được kết hợp với các phương pháp điều trị khác không.
Thuốc opaganib có khả năng trị viêm phổi do COVID-19
Các bệnh nhân nặng bị viêm phổi do COVID-19 được dùng thuốc uống thử nghiệm opaganib, do RedHill Biopharma (Israel) phát triển, cần ít oxy hơn và có thể xuất viện sớm hơn so với bệnh nhân dùng giả dược trong một thử nghiệm ngẫu nhiên nhỏ, các nhà nghiên cứu đã báo cáo vào ngày 29.8 trên medRxiv trước khi được đánh giá ngang hàng.
Trong vòng 14 ngày sau khi tham gia vào nghiên cứu, 50% bệnh nhân COVID-19 dùng opaganib không còn cần oxy, so với 22,2% người trong nhóm dùng giả dược.
Ngoài ra, 86,4% bệnh nhân COVID-19 điều trị bằng opaganib đã được xuất viện, so với 55,6% ở nhóm dùng giả dược.

Hôm 26.8, RedHill Biopharma thông báo rằng opaganib ức chế mạnh mẽ biến thể Delta trong các thí nghiệm trong ống nghiệm. Công ty cho biết loại thuốc này được cho là có tác dụng kháng vi rút bằng cách ức chế sphingosine kinase-2 (SK2), một loại enzym quan trọng trong các tế bào có thể được vi rút tận dụng để hỗ trợ sự nhân lên của nó.
Dựa trên thử nghiệm ban đầu trên 42 bệnh nhân được thực hiện vào năm ngoái, RedHill Biopharma đã đưa ra thử nghiệm ngẫu nhiên lớn hơn nhiều ở những bệnh nhân nhập viện vì viêm phổi nặng do COVID-19.
