Indonesia phát hiện một số siro liên quan tổn thương thận gây tử vong ở trẻ em
Thông tin Y học - Ngày đăng : 11:42, 20/10/2022
Bộ Y tế Indonesia đang điều tra mức tăng đột biến về số ca bệnh và 99 trường hợp tử vong ở trẻ em trong năm nay.
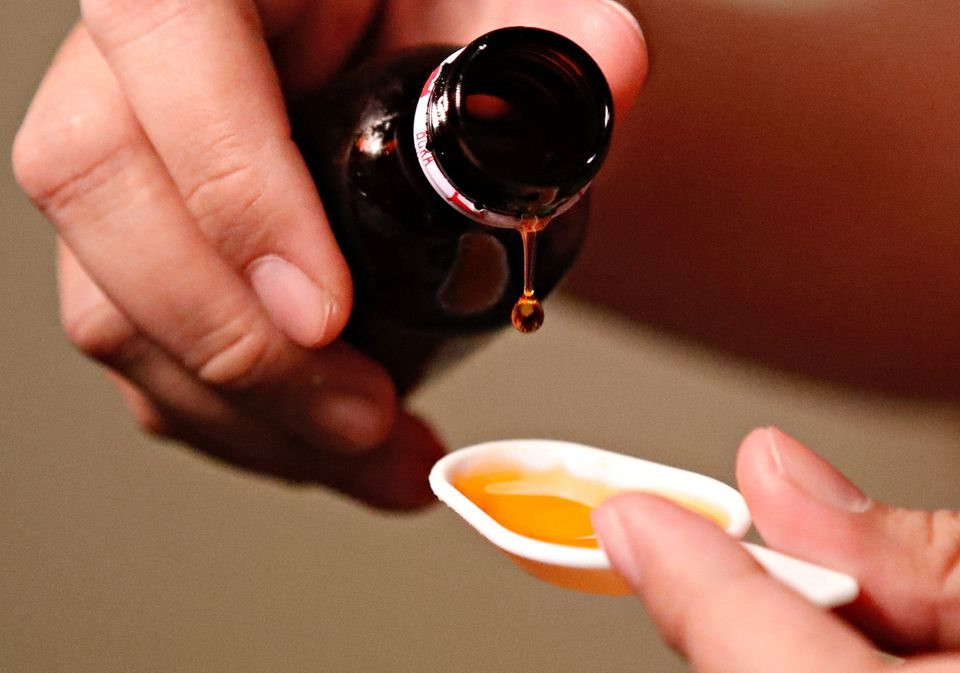
Indonesia đã tạm thời cấm bán tất cả loại thuốc làm từ siro và đang xem xét chặt chẽ các loại siro paracetamol được sử dụng tại địa phương để điều trị sốt cho trẻ em có chứa diethylene glycol và ethylene glycol.
Chính phủ Gambia cũng đang điều tra các trường hợp tử vong do tổn thương thận cấp tính ở trẻ em liên quan đến siro paracetamol. Loại siro này được sản xuất bởi Maiden Pharmaceuticals Ltd có trụ sở tại thủ đô New Delhi, Ấn Độ. Trước đó có 70 trẻ em ở Gambia tử vong liên quan đến siro.
Hôm 20.10, Bộ trưởng Y tế Indonesia - Budi Gunadi Sadikin cho biết ethylene glycol và diethylene glycol đã được phát hiện trong các sản phẩm được tìm thấy tại nhà một số bệnh nhân.
Ông nói: “Một số loại siro mà bệnh nhân tổn thương thận cấp tính dưới 5 tuổi sử dụng đã được chứng minh có chứa ethylene glycol và diethylene glycol mà đáng lẽ không có ở đó, hoặc với số lượng rất ít”.
Tính đến ngày 20.10, Indonesia đã xác định được 206 trường hợp tổn thương thận cấp tính ở trẻ em, trong đó 99 ca tử vong trong năm nay. Ông Budi Gunadi Sadikin nói số trường hợp thực tế có thể cao hơn so với báo cáo.
Người phát ngôn Bộ Y tế Indonesia từ chối cho biết có bao nhiêu bệnh nhân tổn thương thận cấp tính trẻ em mà các thành phần thuốc đã được phát hiện, trích dẫn cuộc điều tra đang diễn ra.
Hôm 12.10, các nhà chức trách y tế Ấn Độ cho biết đã ngừng tất cả việc sản xuất tại Maiden Pharmaceuticals sau khi Tổ chức Y tế Thế giới (WHO) báo cáo rằng siro ho và cảm lạnh xuất khẩu sang Gambia có thể liên quan đến cái chết của 69 trẻ em ở đó.
Được biết đến như một "hiệu thuốc của thế giới", Ấn Độ cung cấp 45% tất cả loại thuốc generic cho châu Phi.
Thuốc generic là bản sao của thuốc biệt dược với thành phần hoạt chất tương tự nhau. Thuốc biệt dược và thuốc generic có hoạt chất và hiệu quả điều trị tương tự. Để có được sự chấp thuận cho đăng ký và bán một loại thuốc, công ty sản xuất cần phải chứng minh rằng thuốc generic có tác dụng tương tự và đáp ứng các tiêu chuẩn cao tương đương thuốc biệt dược. Do đó, quá trình phê duyệt thuốc generic diễn ra rất nghiêm ngặt.
Cái chết của 69 trẻ em ở Gambia - một trong những vụ việc tồi tệ nhất liên quan đến thuốc từ Ấn Độ - đã giáng một đòn mạnh vào ngành công nghiệp có kim ngạch xuất khẩu tăng hơn gấp đôi trong thập kỷ qua, đạt 24,5 tỉ USD trong năm tài chính vừa qua.
Các nhà chức trách Ấn Độ kiểm tra nhà máy chính của Maiden Pharmaceuticals ở bang Haryana bốn lần trong tháng này và cho biết đã đình chỉ tất cả hoạt động sản xuất từ ngày 11.10, sau khi phát hiện công ty này sản xuất và thử nghiệm thuốc vi phạm các quy tắc "trong các hoạt động sản xuất và thử nghiệm".
"Do mức độ nghiêm trọng của các vi phạm quan sát được trong quá trình điều tra và nguy cơ tiềm ẩn của nó với chất lượng, an toàn và hiệu quả loại thuốc được sản xuất, tất cả hoạt động sản xuất của công ty đang bị dừng ngay lập tức", theo lệnh của liên bang và các cơ quan quản lý thuốc bang Haryana.
Naresh Kumar Goyal, Giám đốc điều hành Maiden Pharmaceuticals, từ chối bình luận.
Siro ho và cảm lạnh xuất khẩu sang Gambia được Maiden Pharmaceuticals sản xuất trong một lô duy nhất vào tháng 12.2021 tại nhà máy chính ở quận Sonipat của bang Haryana, khoảng 40 km về phía bắc thủ đô New Delhi, với hạn sử dụng là tháng 11.2024, lệnh cho biết.
Một quan chức y tế hàng đầu Ấn Độ giấu tên nói chính phủ sẽ không dung thứ cho hành vi sai trái nhưng điều quan trọng là phải tìm hiểu chính xác những gì đã xảy ra ở Gambia. Ông phủ nhận cáo buộc của một số nhà phê bình rằng các quy định y tế ở Ấn Độ, đặc biệt là ở cấp bang, là lỏng lẻo.
Chính phủ đã thành lập một ủy ban gồm bốn chuyên gia sẽ tư vấn hành động tiếp theo sau khi "kiểm tra và phân tích các báo cáo về sự kiện bất lợi, mối quan hệ nhân quả và tất cả chi tiết liên quan do WHO chia sẻ".
Luật pháp Ấn Độ cho phép bỏ tù và phạt tiền người bán thuốc giả.
Trợ lý Tổng giám đốc WHO - Mariângela Simão nói trong một cuộc họp báo trực tuyến rằng họ đang hợp tác chặt chẽ với các nhà chức trách Ấn Độ để điều tra về siro ho và cảm lạnh của Maiden Pharmaceuticals. Bà cho biết kết luận từ WHO về những cái chết có liên quan đến thuốc của Maiden Pharmaceuticals dựa trên phân tích một số mẫu thuốc mà trẻ em nhập viện sử dụng.
Maiden Pharmaceuticals cho biết trên trang web của mình rằng hãng có công suất sản xuất hàng năm là 2,2 triệu chai siro, 600 triệu viên nang, 18 triệu thuốc dạng tiêm, 300.000 ống thuốc mỡ và 1,2 tỉ viên nén tại các nhà máy ở bang Haryana. Maiden Pharmaceuticals có hai nhà máy khác trong bang Haryana ngoài nhà máy chính.
WHO đã đưa ra một cảnh báo sản phẩm y tế, yêu cầu các cơ quan quản lý loại bỏ siro ho và cảm lạnh của Maiden Pharmaceuticals khỏi thị trường.
Cơ quan y tế Liên Hợp Quốc cho biết phân tích trong phòng thí nghiệm với bốn sản phẩm Maiden Pharmaceuticals (Promethazine Oral Solution, Siro Kofexmalin Baby Cough, Siro Makoff Baby Cough Syrup và Siro Magrip N Cold) có lượng diethylene glycol và ethylene glycol, có thể gây hại và dẫn đến tổn thương thận cấp tính.
Diethylene glycol và ethylene glycol được sử dụng như chất thay thế rẻ hơn trong một số sản phẩm dược phẩm cho glycerine, một dung môi hoặc chất làm đặc trong nhiều loại siro ho.
Trong một báo cáo điều tra sơ bộ hôm 11.10, Cảnh sát Gambia nói rằng cái chết của 69 trẻ em do tổn thương thận cấp tính có liên quan đến siro ho được sản xuất tại Ấn Độ và nhập khẩu qua Atlantic Pharmaceuticals. Atlantic Pharmaceuticals từ chối bình luận về vấn đề này.
Ấn Độ cho biết siro ho chỉ được phép xuất khẩu sang Gambia, dù WHO cho biết chúng có thể đã đến nơi khác thông qua các thị trường không chính thức.
