Ngày 1.9, hãng dược Moderna đã nộp đơn xin cấp phép liều vắc xin tăng cường lên Cơ quan Quản lý Thực phẩm và Dược phẩm Mỹ (FDA).
Cơ quan Quản lý thực phẩm và dược phẩm Mỹ (FDA) Mỹ đã phê duyệt tiêm vắc xin ngừa COVID-19 bổ sung cho người bị tổn thương hệ miễn dịch. Sẽ dùng vắc xin của Pfizer và Moderna.
Ngày 1.9, cơ quan này cho biết một nhóm cố vấn của họ sẽ thảo luận về việc phê duyệt mũi vắc xin tăng cường của Pfizer vào ngày 17.9, nhưng không rõ liệu họ có thảo luận về vắc xin Moderna hay không.
Moderna cho biết họ đã gửi dữ liệu ban đầu về việc sử dụng mũi vắc xin tăng cường 50 microgram trong loại vắc xin tiêm 2 mũi của mình. Vắc xin Moderna ban đầu chứa 100 microgram mRNA trong mỗi mũi tiêm.
Giám đốc điều hành Moderna, Stéphane Bancel cho biết trong một tuyên bố rằng người nhận liều 50 microgram có phản ứng kháng thể mạnh mẽ chống lại biến chủng Delta.

Mặc dù Moderna đã nói rằng vắc xin COVID-19 của họ vẫn còn hiệu quả khoảng 93% trong 6 tháng sau mũi tiêm thứ 2, nhưng theo quan sát họ thấy rằng mức độ kháng thể đã suy yếu đáng kể vào thời điểm đó.
Moderna cho biết gần 350 người tham gia thử nghiệm giai đoạn II ban đầu đã được tiêm mũi vắc xin tăng cường tạo ra phản ứng miễn dịch tốt hơn so với những gì đã thấy sau mũi tiêm thứ 2 trong thử nghiệm lâm sàng lớn ở giai đoạn III.
Moderna cho biết tính an toàn của liều vắc xin tăng cường tương tự như liều thứ 2. Họ cũng dự kiến sẽ gửi dữ liệu lên Cơ quan Dược phẩm Châu Âu (EMA) và các cơ quan quản lý khác trên thế giới trong những ngày tới.
Một số quốc gia đã triển khai kế hoạch tiêm mũi vắc xin tăng cường cho những người lớn tuổi, những người bị tổn thương hệ miễn dịch và những người có mức độ kháng thể suy giảm sau 6 tháng tiêm chủng.
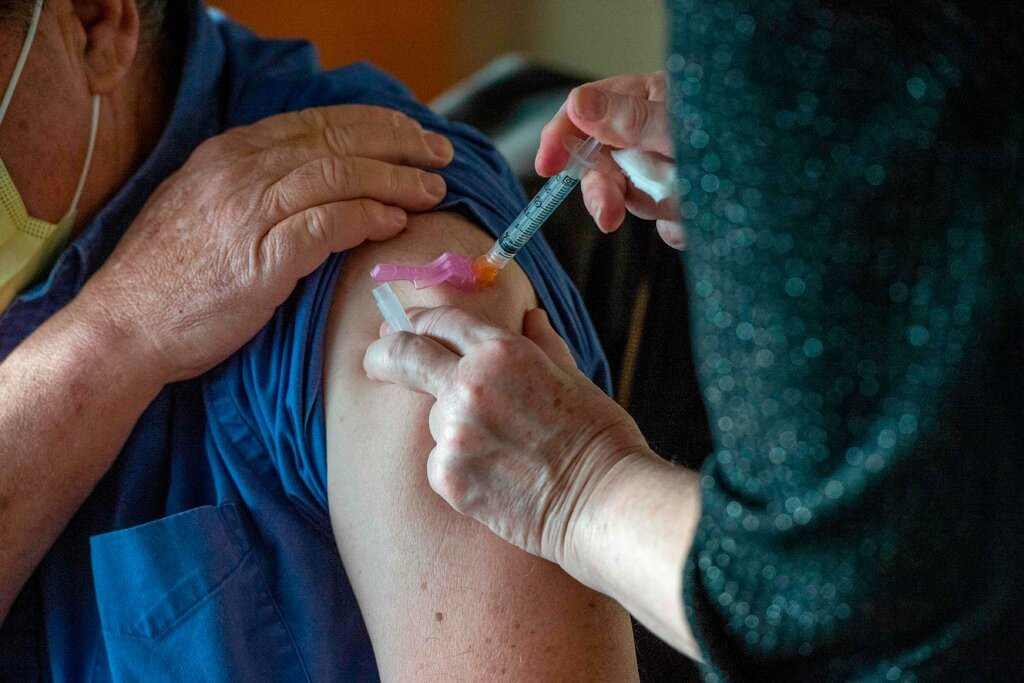
Trước đó, Chính phủ Mỹ thông báo sẽ tiêm mũi vắc xin tăng cường cho người dân Mỹ từ ngày 20.9, với điều kiện họ đã tiêm đủ hai liều vắc xin từ 8 tháng trước đó.
Giới chức Mỹ cho biết họ sẽ bắt đầu chương trình tiêm bổ sung sau khi FDA và CDC quyết định mũi vắc xin tăng cường là cần thiết.