Hôm 21.12, AstraZeneca cho biết họ đang làm việc với Đại học Oxford (Anh) để sản xuất loại vắc xin nhắm vào biến thể Omicron.
Như vậy, hãng dược Anh – Thụy Điển sẽ cùng các nhà sản xuất khác tìm cách phát triển vắc xin dành riêng cho Omicron.
Người phát ngôn của AstraZeneca cho biết: “Cùng với Đại học Oxford, chúng tôi đã thực hiện các bước sơ bộ trong việc sản xuất vắc xin biến thể Omicron trong trường hợp cần thiết và sẽ thông báo bằng các dữ liệu mới”.
Tờ Financial Times lần đầu tiên đưa tin này, trích lời Sandy Douglas, trưởng nhóm nghiên cứu tại Đại học Oxford.
Sandy Douglas nói với Financial Times: “Về nguyên tắc, vắc xin dựa trên adenovirus (chẳng hạn như vắc xin do Oxford - AstraZeneca sản xuất) có thể được sử dụng để đáp ứng với bất kỳ biến thể mới nào nhanh hơn so với một số loại trước đây”.
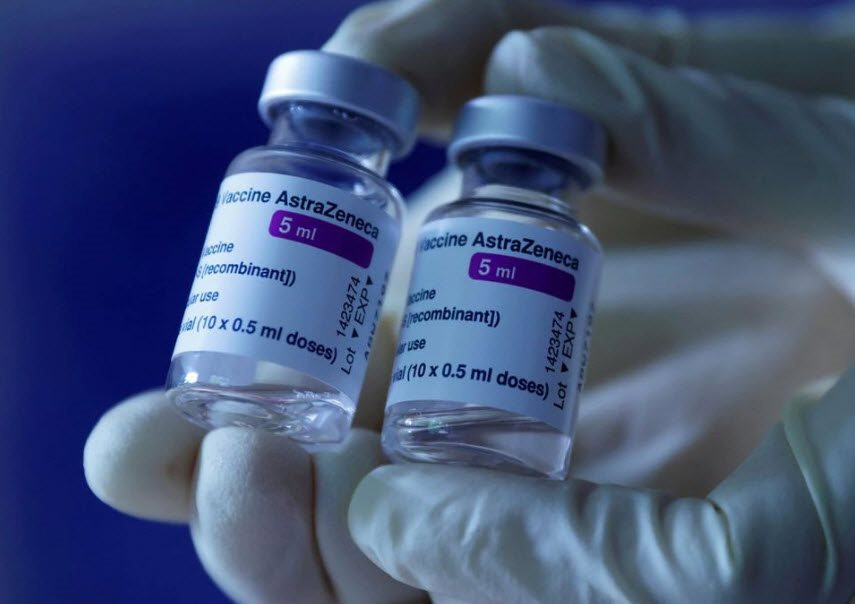
Một nghiên cứu trong phòng thí nghiệm vào tuần trước phát hiện hỗn hợp kháng thể Evusheld của AstraZeneca vẫn giữ được hoạt tính trung hòa chống lại biến thể Omicron.
Nghiên cứu được thực hiện bởi các nhà điều tra độc lập của Cục Quản lý Thực phẩm và Dược phẩm Mỹ (FDA).
AstraZeneca nói thêm rằng nhiều phân tích hơn về Evusheld chống lại Omicron đang được tiến hành bởi công ty và các bên thứ ba, với dữ liệu dự kiến có rất sớm.
Hôm 18.11, hãng dược Anh – Thụy Điển cho biết Evusheld sẽ cung cấp khả năng bảo vệ 83% trước COVID-19 trong vòng 6 tháng.
Theo AstraZeneca một nghiên cứu riêng biệt ở những bệnh nhân COVID-19 từ nhẹ đến trung bình cho thấy liều Evusheld cao hơn giúp giảm 88% nguy cơ phát bệnh tồi tệ hơn khi được sử dụng trong vòng 3 ngày kể từ khi có triệu chứng đầu tiên.
Evusheld làm giảm một nửa nguy cơ mắc COVID-19 nghiêm trọng hoặc tử vong ở những bệnh nhân không nhập viện đã có các triệu chứng từ 7 ngày trở xuống trong một thử nghiệm giai đoạn muộn, được công bố ngày 11.10.
Trước đó, Pfizer – BioNTech và Moderna cũng cho biết đang nghiên cứu vắc xin COVID-19 đặc trị Omicron.
Moderna hy vọng sẽ bắt đầu thử nghiệm lâm sàng vắc xin này vào đầu năm tới.
WHO khuyến cáo tiêm liều vắc xin Novavax thứ 3 cho người có vấn đề về sức khỏe
Hôm 21.2, Novavax (Mỹ) cho biết ban chuyên gia của Tổ chức Y tế Thế giới (WHO) đã khuyến nghị tiêm liều thứ ba vắc xin NVX-CoV2373 của họ cho những người bị suy giảm miễn dịch.
Nhóm cố vấn chiến lược của WHO gồm các chuyên gia về tiêm chủng (được gọi là SAGE) đưa ra một loạt khuyến nghị, bao gồm cả việc sử dụng vắc xin COVID-19 công nghệ protein tái tổ hợp này ở những người mắc bệnh nền, phụ nữ đang cho con bú và những người sống chung với HIV.
Sau khi xem xét dữ liệu của Novavax, các chuyên gia độc lập cho biết vắc xin này có thể được sử dụng cho phụ nữ mang thai nếu lợi ích của việc tiêm phòng cho họ lớn hơn những rủi ro có thể xảy ra.
Hôm 17.12, WHO đã cấp phép sử dụng khẩn cấp vắc xin của Novavax do Viện Huyết thanh Ấn Độ sản xuất, mở đường cho việc sử dụng nó ở các quốc gia có thu nhập thấp và trung bình, nơi việc triển khai tiêm chủng chậm hơn nhiều so với châu Âu.
Đây là vắc xin COVID-19 thứ 9 được WHO phê duyệt sau Pfizer - BioNTech, Moderna (cùng công nghệ mRNA); AstraZeneca, Covishield (phiên bản AstraZeneca sản xuất ở Ấn Độ), Johnson & Johnson (cùng công nghệ vector vi rút); Bharat Biotech, Sinovac Biotech và Sinopharm (cùng công nghệ bất hoạt).
Hôm 20.12, Ủy ban châu Âu đã phê duyệt sử dụng khẩn cấp vắc xin COVID-19 của Novavax (dưới tên gọi Nuvaxovid) ở Liên minh châu Âu (EU).
Chủ tịch Ủy ban châu Âu, bà Ursula von der Leyen, cho biết: “Với 5 loại vắc xin đã được phê duyệt, EU có một danh mục đầu tư đa dạng, dựa trên cả công nghệ mới, chẳng hạn mRNA, và những công nghệ cổ điển như Novavax, dựa trên protein”.
Quyết định này được đưa ra ngay sau khi Cơ quan quản lý dược phẩm châu Âu (EMA) khuyến nghị phê duyệt vắc xin này.
"Sau khi đánh giá kỹ lưỡng, Ủy ban dược phẩm cho con người của EMA nhất trí rằng dữ liệu về vắc xin này mạnh và đáp ứng đầy đủ các tiêu chí của EU về hiệu quả, an toàn và chất lượng", EMA thông báo.
Nuvaxovid là vắc xin COVID-19 thứ 5 được cấp phép sử dụng khẩn cấp tại châu Âu sau Moderna, Pfizer-BioNTech, AstraZeneca và Johnson & Johnson.
Công ty công nghệ sinh học Mỹ cũng cho biết đã bắt đầu sử dụng những liều tăng cường đầu tiên của NVX-CoV2373 trong thử nghiệm giai đoạn cuối.
Hôm 2.12, Novavax thông báo có thể bắt đầu sản xuất thương mại vắc xin COVID-19 được điều chỉnh đối phó Omicron vào tháng 1.2022, đồng thời kiểm tra xem vắc xin hiện tại có hoạt động chống lại biến thể này không.
Dữ liệu phòng thí nghiệm dự kiến trong những tuần tới sẽ cho thấy các kháng thể từ những cá nhân trước đó đã được tiêm vắc xin COVID-19 của Novavax có thể vô hiệu hóa Omicron không, theo công ty công nghệ sinh học Mỹ.
Novavax cũng hé lộ đã bắt đầu phát triển một kháng nguyên protein gai đặc trị Omicron và sẽ bắt đầu các thử nghiệm trong phòng thí nghiệm một loại vắc xin mới để nhắm mục tiêu biến thể này vài tuần nữa.