Cục Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) hôm 20.10 đã phê duyệt liều tăng cường của vắc xin COVID-19 từ Moderna và Johnson & Johnson, đồng thời cho biết người Mỹ có thể chọn vắc xin khác với loại ban đầu để tiêm nhắc lại.
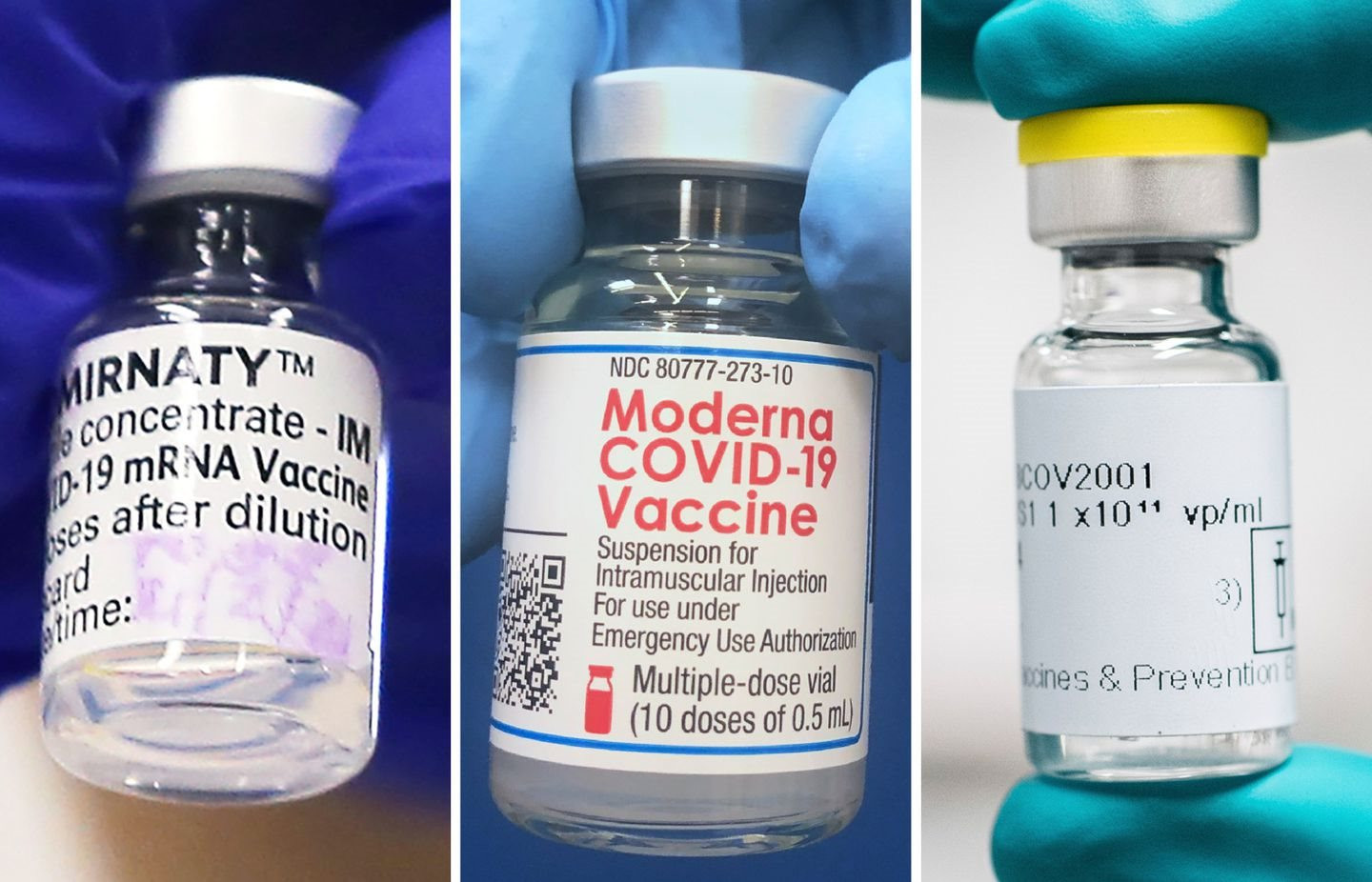
Điều đó có nghĩa là cả ba loại vắc xin FDA phê duyệt tại Mỹ đều có thể được sử dụng làm liều tăng cường cho một số nhóm.
"Sự sẵn có của các liều vắc xin tăng cường được phê duyệt này là rất quan trọng để tiếp tục bảo vệ chống lại bệnh COVID-19", Ủy viên FDA - Janet Woodcock cho biết. Bà lưu ý rằng dữ liệu cho thấy hiệu quả của vắc xin có thể giảm dần theo thời gian ở một số người được tiêm chủng đầy đủ.
Quyết định này mở đường cho hàng triệu người ở Mỹ có được sự bảo vệ bổ sung vì biến thể Delta rất dễ lây lan gây ra các ca nhiễm trùng đột phá ở một số người đã tiêm 2 mũi vắc xin.
FDA trước đây đã phê duyệt liều tăng cường vắc xin COVID-19 của Pfizer - BioNTech SE ít nhất 6 tháng sau đợt tiêm đầu tiên để tăng cường bảo vệ cho những người từ 65 tuổi trở lên, những ai có nguy cơ mắc bệnh nặng và những người thường xuyên tiếp xúc với vi rút do công việc của họ.
Tuần trước, một ban cố vấn cho FDA đã bỏ phiếu đề nghị tiêm mũi vắc xin Moderna thứ ba cho các nhóm tương tự. Liều vắc xin Moderna tăng cường dùng một nửa sức mạnh so với mũi tiêm ban đầu của công ty (50 microgram so với 100 microgram).
Ban hội thẩm cũng khuyến nghị tiêm mũi thứ hai của vắc xin Johnson & Johnson cho tất cả những người từng nhận vắc xin này hai tháng trước đó.
Tuần trước, các quan chức FDA cho biết đang xem xét giảm độ tuổi khuyến cáo tiêm liều tăng cường vắc xin Pfizer - BioNTech xuống từ 40 tuổi, dựa trên dữ liệu từ Israel, nơi các mũi tiêm nhắc lại vắc xin này được sử dụng rộng rãi và phát huy hiệu quả.
FDA chưa hạ độ tuổi cho liều vắc xin Pfizer - BioNTech tăng cường, nhưng cho biết họ đang đánh giá những lợi ích và rủi ro của việc sử dụng rộng rãi hơn liều thứ ba rồi có kế hoạch cập nhật cho công chúng những tuần tới.
"Có bằng chứng cho thấy khả năng giảm tuổi của những người đủ điều kiện nhận liều văng xin tăng cường có thể có ý nghĩa trong tương lai. Đó là thứ mà chúng tôi đang xem xét kỹ lưỡng", quan chức FDA - Peter Marks phát biểu trong một cuộc họp báo.
'Hỗn hợp và phối hợp'
FDA và Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh Mỹ (CDC) đã phải chịu áp lực để cho phép các mũi tiêm bổ sung sau khi Nhà Trắng công bố kế hoạch vào tháng 8 cho một chiến dịch vắc xin tăng cường rộng rãi.
Cuộc họp của ban cố vấn bao gồm phần trình bày dữ liệu về việc trộn vắc xin từ nghiên cứu của Viện Y tế Quốc gia Mỹ, trong đó 458 người tham gia đã nhận được một số mũi tiêm kết hợp Pfizer - BioNTech, Moderna và Johnson & Johnson.
Dữ liệu cho thấy những người ban đầu tiêm vắc xin COVID-19 của Johnson & Johnson có đáp ứng miễn dịch mạnh hơn khi được tăng cường bằng liều Pfizer hoặc Moderna và rằng mũi tiêm tăng cường kết hợp với loại vắc xin khác là an toàn ở người lớn. Xem chi tiết tại đây.
Tuy nhiên, các quan chức FDA cho biết dữ liệu vẫn chưa rõ ràng về việc liệu có nên ưu tiên tiêm liều tăng cường khác loại vắc xin ban đầu hay không.
Nhiều quốc gia bao gồm cả Anh đã ủng hộ các chiến lược tiêm kết hợp với vắc xin AstraZeneca vốn được sử dụng rộng rãi. Loại vắc xin này không được cấp phép ở Mỹ nhưng dựa trên công nghệ vectơ vi rút tương tự như Johnson & Johnson.
Reuters đưa tin vào tháng 6 rằng các chuyên gia về bệnh truyền nhiễm đang cân nhắc nhu cầu tiêm nhắc lại vắc xin Pfizer hoặc Moderna sau khi nhận liều Johnson & Johnson (loại 1 mũi).
Một ủy ban cố vấn của CDC vào ngày 21.10 sẽ đưa ra khuyến nghị về những nhóm người nào nên nhận liều tăng cường của vắc xin Moderna và Johnson & Johnson, mà giám đốc cơ quan sẽ sử dụng để thông báo quyết định cuối cùng.
Theo dữ liệu từ CDC, khoảng 11,2 triệu người Mỹ đến nay đã được tiêm liều vắc xin COVID-19 thứ ba.